 |
3M�h����˹�ؾ��yԇƬ�����Լ����x | ||
| һ���yԇ�h����˹�ؾ��� �������� | |||
 1. ��δ�_��ĜyԇƬ�A����<= 8 oC (46 oF)�ĭh���£����ڰ��b�Ϙ�ʾ����Ч�ڃ�ʹ�á��ڸߝ�ȵĵط��������ʹ��ǰ���yԇƬ�؏͵��Ҝء� 1. ��δ�_��ĜyԇƬ�A����<= 8 oC (46 oF)�ĭh���£����ڰ��b�Ϙ�ʾ����Ч�ڃ�ʹ�á��ڸߝ�ȵĵط��������ʹ��ǰ���yԇƬ�؏͵��Ҝء� |
 2. ���_��ĜyԇƬ�����_�ڷ��ۣ����z����á� 2. ���_��ĜyԇƬ�����_�ڷ��ۣ����z����á� |
||
 3. ���ֹ��¶�ڳ���ĭh���У�Ո��Ҫ������_��ĜyԇƬ�����z����õĜyԇƬ�A���ڵ͜ظ���ĵط������֕r�g�����^1���¡�Ո�����yԇƬ���ڜض�> 25 oC (77 oF)��(��)�������> 50%�ĭh���С� 3. ���ֹ��¶�ڳ���ĭh���У�Ո��Ҫ������_��ĜyԇƬ�����z����õĜyԇƬ�A���ڵ͜ظ���ĵط������֕r�g�����^1���¡�Ո�����yԇƬ���ڜض�> 25 oC (77 oF)��(��)�������> 50%�ĭh���С� |
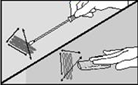 4. ��ͿĨ�������������ɘ��O���ռ��h���ӱ����ɘ��O���Һ�w��<= 10 mL���������ǟo��ˮ�����_������ˮ(Buffered Peptone Water, BPW)�����к;��_Һ����Letheen�✫��Dey/Engley (DE)�к��✫�� 4. ��ͿĨ�������������ɘ��O���ռ��h���ӱ����ɘ��O���Һ�w��<= 10 mL���������ǟo��ˮ�����_������ˮ(Buffered Peptone Water, BPW)�����к;��_Һ����Letheen�✫��Dey/Engley (DE)�к��✫�� |
||
 5. �ڟo���h�������ռ��Ę�Ʒ������5 mL��20-30oC�����^���ľ��_������ˮ(BPW)��Һ�� ��Ҫ��Petrifilm EL�yԇƬ�cVermont ���B��(UVM)��Fraser�✫����˹�ؾ��������B�� (LEB)�_��˹�ؾ��������B��(BLEB)���á� 5. �ڟo���h�������ռ��Ę�Ʒ������5 mL��20-30oC�����^���ľ��_������ˮ(BPW)��Һ�� ��Ҫ��Petrifilm EL�yԇƬ�cVermont ���B��(UVM)��Fraser�✫����˹�ؾ��������B�� (LEB)�_��˹�ؾ��������B��(BLEB)���á� |
 6. ��ϣ���ӻ����D��Ʒ�cBPW�Ļ��Һ����һ��犡�����Ʒ�����Ҝ�(20-30 oC) 1h����ò����^1.5 h�����ޏ͓p������˹�ؾ��� 6. ��ϣ���ӻ����D��Ʒ�cBPW�Ļ��Һ����һ��犡�����Ʒ�����Ҝ�(20-30 oC) 1h����ò����^1.5 h�����ޏ͓p������˹�ؾ��� |
||
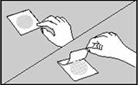 7. ���yԇƬ����ƽ̹����̎�����_�ό�Ĥ�� 7. ���yԇƬ����ƽ̹����̎�����_�ό�Ĥ�� |
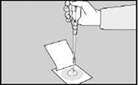 8. ��3MTM�����Һ����������Һ����ֱ�μ�3 mL��Ʒ����Ĥ�����롣 8. ��3MTM�����Һ����������Һ����ֱ�μ�3 mL��Ʒ����Ĥ�����롣 |
||
 9. ���ό�Ĥ�����w�£�����a�����ݡ� 9. ���ό�Ĥ�����w�£�����a�����ݡ� |
 10. �p�p�،����ω������λ�ڽӷN�^�ό�Ĥ�ϡ���Ҫ����Ť�D�Ӊ��塣�������塣������10��犣���ʹ�z�w���̡� 10. �p�p�،����ω������λ�ڽӷN�^�ό�Ĥ�ϡ���Ҫ����Ť�D�Ӊ��塣�������塣������10��犣���ʹ�z�w���̡� |
||
 11. ���yԇƬ���泯�ϣ��ɯB����10Ƭ����35oC ± 1oC��37oC ± 1oC�����B28h ± 2 h�� 11. ���yԇƬ���泯�ϣ��ɯB����10Ƭ����35oC ± 1oC��37oC ± 1oC�����B28h ± 2 h�� |
 12. Petrifilm EL�yԇƬ�܉��ؘʵľ���Ӌ������������W�Ŵ���Ӌ�������x����ҪӋ���A��݆���ϵľ��䣬������������x�������B�������á� 12. Petrifilm EL�yԇƬ�܉��ؘʵľ���Ӌ������������W�Ŵ���Ӌ�������x����ҪӋ���A��݆���ϵľ��䣬������������x�������B�������á� |
||
|
Petrifilm EL�yԇƬ�������ڶ��ԡ��붨���������z�y
|
|||
 |
 |
13. ���ڶ��ԙz�y�������ϼtɫ����Ĵ����c���Y��Ӌ��z����δ�z���� �����/��ĽY���ѽ��܉�M����Ҫ����ô������x���ԙz�y�� |
 14. ���ڰ붨���z�y���������F�ϼtɫ�������������ӛ䛽Y���� ������Ǹ������䔵��������������ȡ�����Ĵ�ʩ�����қ]��Ҫӛ䛌��H���䔵����ô������x��붨���z�y����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���) 14. ���ڰ붨���z�y���������F�ϼtɫ�������������ӛ䛽Y���� ������Ǹ������䔵��������������ȡ�����Ĵ�ʩ�����қ]��Ҫӛ䛌��H���䔵����ô������x��붨���z�y����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���) |
|
δ�z��
|
�z��
|
||
 15. ���ڶ����z�y��Ӌ�������ϼtɫ���䡣 �����������䔵����ȡ�����Ĵ�ʩ������Բ��ö����z�y���yԇƬ����˹�ؾ�����16 15. ���ڶ����z�y��Ӌ�������ϼtɫ���䡣 �����������䔵����ȡ�����Ĵ�ʩ������Բ��ö����z�y���yԇƬ����˹�ؾ�����16Ո�������x�փԵ�“�����ɘ��c���x”���ց�Ӌ��ÿ���h���ӱ��е���˹�ؾ����� |
 16. ����^�����M���Mһ���b���������ό�Ĥ�����z����ȡ���䡣 16. ����^�����M���Mһ���b���������ό�Ĥ�����z����ȡ���䡣 |
||
|
�����ɘ��c���x
|
|||
|
������Զ�����ʽʹ��3M Petrifilm EL �yԇƬ��Ո�����aƷ�İ��b�����Ȼ��������ʽӋ���λ��e�ľ��䔵(Colony Forming Units, CFU)��ͬ�r����ҲҪע�������c�� 1.���������ڭh���O���^���Ы@��������Ϣ���P�I�c�������ڲɘ��^���Б�ʹ����ͬ�IJ��E��������r�£���ʹ����ͬ��͵�ȡ���O�䣬ģ����e�����g�T�ͲɘӼ��g�� ���˜y����λ�ɘ���e����˹�ؾ���������Ҫӛ��������� |
|||
|
|
|||
|
��
 |
|||
| �h�������ɘӷ��������īI�� Standard Methods for the Examination of Dairy Products, Section 3.7D, American Public Health Association, Washington D. C., 1992. Compendium of Methods for the Microbiological Examination of Foods, Section 3.512 and 3.521, American Public Health Association, Washington D. C., 2001 |
|||
|
�������x
|
|||
 1. ��10 mLҺ�w���d��ͿĨ�ɘ��棬����e��1ƽ��Ӣ��(1 ft2)�� 1. ��10 mLҺ�w���d��ͿĨ�ɘ��棬����e��1ƽ��Ӣ��(1 ft2)�� |
 2. �����d�Ż؟o������������5 mL���_������ˮ(BPW)�� 2. �����d�Ż؟o������������5 mL���_������ˮ(BPW)�� |
||
 3. �ޏ���ɺ���ȡ3 mL���Һ�ӷN��Petrifilm EL�yԇƬ�� 3. �ޏ���ɺ���ȡ3 mL���Һ�ӷN��Petrifilm EL�yԇƬ�� |
 4. ���B���M�о���Ӌ�� (�ڱ����У����O���䔵��90)�� 4. ���B���M�о���Ӌ�� (�ڱ����У����O���䔵��90)�� |
||
 |
|||
 1. ��1 mLҺ�w��ͿĨ�^��ͿĨ�ɘ��棬����e��50ƽ������(50 cm2). 1. ��1 mLҺ�w��ͿĨ�^��ͿĨ�ɘ��棬����e��50ƽ������(50 cm2). |
 2. ��ͿĨ���Ż؟o�������У�����5 mL���_������ˮ(BPW)�� 2. ��ͿĨ���Ż؟o�������У�����5 mL���_������ˮ(BPW)�� |
||
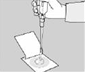 3. �ޏ���ɺ���ȡ3 mL���Һ�ӷN��Petrifilm EL �yԇƬ�� 3. �ޏ���ɺ���ȡ3 mL���Һ�ӷN��Petrifilm EL �yԇƬ�� |
 4. ���B���M�о���Ӌ�� (�ڱ����У�������䔵��90)�� 4. ���B���M�о���Ӌ�� (�ڱ����У�������䔵��90)�� |
||
 |
|||
| �����yԇ�h����˹�ؾ� ���x���� | |||
| 3MTM PetrifilmTM Environmental Listeria(EL) �yԇƬ��һ�N�A���Ƃ�õ����B���������x����ԇ�����I�B�ɷ֣���ˮ�����Ե����z�������ھ���z�y���@ɫָʾ����Petrifilm EL �yԇƬ�����ڙz�y��Ӌ���h���ӱ��е���˹�ؾ�����Petrifilm EL �yԇƬ�z�y����˹�ؾ������κ�������˹�ؾ�(L.monocytogenes) Ӣ�Z����˹�ؾ� (L.innocua)������/ī����˹�ؾ�(L.grayi/murrayi)��������˹�ؾ�(L.welshimeri)�������܅^�ָ��N���� �h���l�������������ܕ����ƻ�p��������_�����˾��_Һ(Buffered Peptone Water, BPW) �������ޏ��✫��Petrifilm EL�yԇƬ�Y��ʹ�á�����˹�ؾ��ھ��浰���˾��_Һ�е��ޏ��^�̲����������E�� |
|||
 1. �D1 ���L����˹�ؾ��ĵ���Petrifilm EL �yԇƬ�����x��Ӌ�����е��ϼtɫ�������˹�ؾ��������26-29 С�r���л�ɫ�ۼtɫ������ڣ����^�m���B�������B�r�g�ȣ��ɻ�ɫ�ۼtɫ������ϼtɫ�ľ��䑪�ж�����˹�ؾ�����������B�r�g(30С�r)�Ա��ֻ�ɫ�ۼtɫ�ľ��䲻�����x����˹�ؾ��������]��Ӌ���A��݆���ϵľ��䣬������������x�������B�������á� 1. �D1 ���L����˹�ؾ��ĵ���Petrifilm EL �yԇƬ�����x��Ӌ�����е��ϼtɫ�������˹�ؾ��������26-29 С�r���л�ɫ�ۼtɫ������ڣ����^�m���B�������B�r�g�ȣ��ɻ�ɫ�ۼtɫ������ϼtɫ�ľ��䑪�ж�����˹�ؾ�����������B�r�g(30С�r)�Ա��ֻ�ɫ�ۼtɫ�ľ��䲻�����x����˹�ؾ��������]��Ӌ���A��݆���ϵľ��䣬������������x�������B�������á��������x�� �yԇƬ�z����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x�� �yԇƬ�ϵ���˹�ؾ�����11�� Ո�������x�փԵ�“�����ɘ��c���x”���ց�Ӌ��ÿ���h���ӱ��е���˹�ؾ����� |
 2. ԓPetrifilm EL �yԇƬ�����B30С�r��]�о������L�����Y���� 2. ԓPetrifilm EL �yԇƬ�����B30С�r��]�о������L�����Y�����������x�� �yԇƬ��δ�z����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x���yԇƬ�ϵ���˹�ؾ�����< 1�� Ո�������x�փԵ�“�����ɘ��c���x”���ց�Ӌ��ÿ���h���ӱ��е���˹�ؾ����� |
||
 3. Petrifilm EL�yԇƬ����˹�ؾ������x���ԣ�������@ʾ���ϼtɫ�� 3. Petrifilm EL�yԇƬ����˹�ؾ������x���ԣ�������@ʾ���ϼtɫ���������x�� �yԇƬ�ϙz����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x���yԇƬ�ϵ���˹�ؾ�����84 �� Ո�������x�փԵ�“�����ɘ��c���x”���ց�Ӌ��ÿ���h���ӱ��е���˹�ؾ����� |
 4. ����Petrifilm EL�yԇƬ�����x��ʽ�����N�����ԛ]�н��h��Ӌ���������������ܼ��r�������·�ʽ���x���Ի�붨���ĽY��������㶨���ĽY���� 4. ����Petrifilm EL�yԇƬ�����x��ʽ�����N�����ԛ]�н��h��Ӌ���������������ܼ��r�������·�ʽ���x���Ի�붨���ĽY��������㶨���ĽY�����������x���yԇƬ�ϙz����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x���yԇƬ�Ϲ������˹�ؾ������s460����������˹�ؾ����ڕr��ͨ�^Ӌ���ɂ���ɂ����ϵľ��д����Է���ľ��䔵�����㡣Ӌ��ÿ�������ƽ�����䔵�������42��Petrifilm EL�yԇƬ�ĽӷN��e����42 cm2�� |
||
 5. �����䔵�ܶ��r���yԇƬ�Ͽ������S��С�ģ�������ľ��䣬��(��) �ʬFȫ���ķۼtɫ����ɫ�� 5. �����䔵�ܶ��r���yԇƬ�Ͽ������S��С�ģ�������ľ��䣬��(��) �ʬFȫ���ķۼtɫ����ɫ���������x���yԇƬ�ϙz����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x���yԇƬ�ϵ���˹�ؾ�������Ӌ(Too Numerous To Count, TNTC)��ԓ�D�еľ��䔵����104�� |
 6. �����ɫ���ܕ����h���ӱ��еĻ҉m��������ɰ�ӡ���������������l��׃����Ҳ���������ɘ��O���(��) ���_������ˮ(�ޏ�Һ)��Ʒ�Ʋ�ͬ�������ϼtɫ�������x����˹�ؾ��� 6. �����ɫ���ܕ����h���ӱ��еĻ҉m��������ɰ�ӡ���������������l��׃����Ҳ���������ɘ��O���(��) ���_������ˮ(�ޏ�Һ)��Ʒ�Ʋ�ͬ�������ϼtɫ�������x����˹�ؾ����������x���yԇƬ�ϙz����˹�ؾ��� �붨�����x����˹�ؾ��ĺ�����ӛ䛞錦�ɘӅ^�����I�˜���ָ�����x����ʽ(��ͣ��У��ߣ���ɽ��ܺͲ��ɽ���)�� �������x���yԇƬ�ϵ���˹�ؾ�����11�� Ո�������x�փԵ�“�����ɘ��c���x”���ց�Ӌ��ÿ���h���ӱ��е���˹�ؾ����� |
||
 �֙C��
�֙C��






